 Диаграмма пурбе для никеля. Хром +6 в щелочной среде. Fe ph 3. Углы связи в молекуле ph3. Fe ph 3.
Диаграмма пурбе для никеля. Хром +6 в щелочной среде. Fe ph 3. Углы связи в молекуле ph3. Fe ph 3.
|
 Fe ph 3. Fe ph 3. Диаграмма пурбе для никеля. Хром в кислой среде щелочной нейтральной. Hcl уравнение реакции.
Fe ph 3. Fe ph 3. Диаграмма пурбе для никеля. Хром в кислой среде щелочной нейтральной. Hcl уравнение реакции.
|
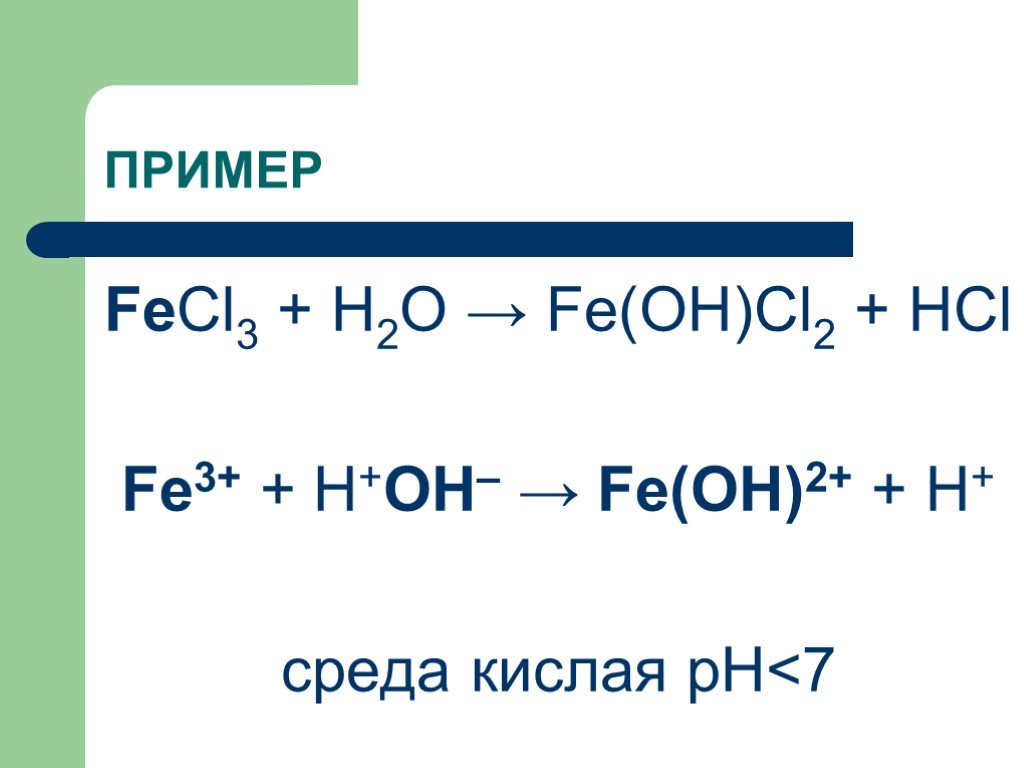
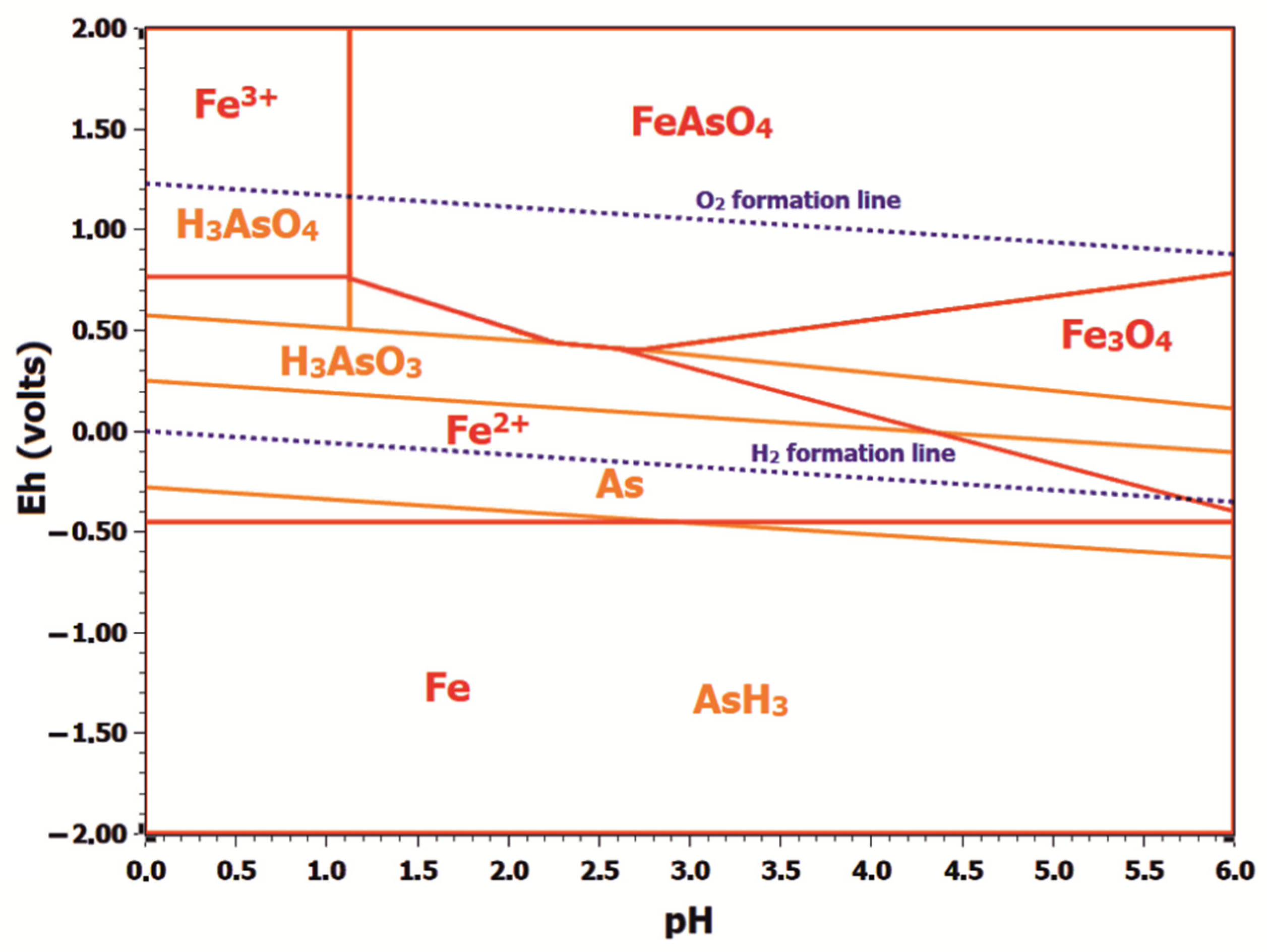 Fe ph 3. Fe ph 3. Раствор соляной кислоты это ph=7. Уравнение гидролиза хлорида железа 3. Кдж/моль.
Fe ph 3. Fe ph 3. Раствор соляной кислоты это ph=7. Уравнение гидролиза хлорида железа 3. Кдж/моль.
|
 Fe 2 соединения. Fe ph 3. Ph fe. Fe+fecl3+h2o. Ag+hno3.
Fe 2 соединения. Fe ph 3. Ph fe. Fe+fecl3+h2o. Ag+hno3.
|
 Диаграмма пурбе железо. Fe ph 3. Ph na2co3 аналитика. Fe ph 3. Fe ph 3.
Диаграмма пурбе железо. Fe ph 3. Ph na2co3 аналитика. Fe ph 3. Fe ph 3.
|
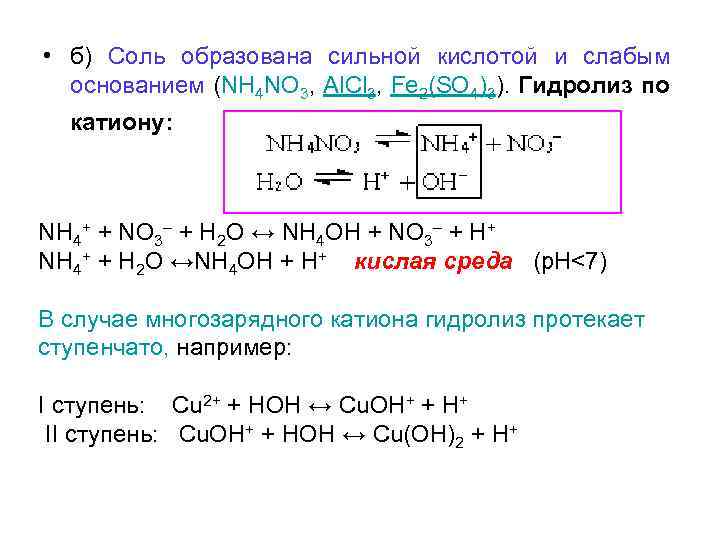
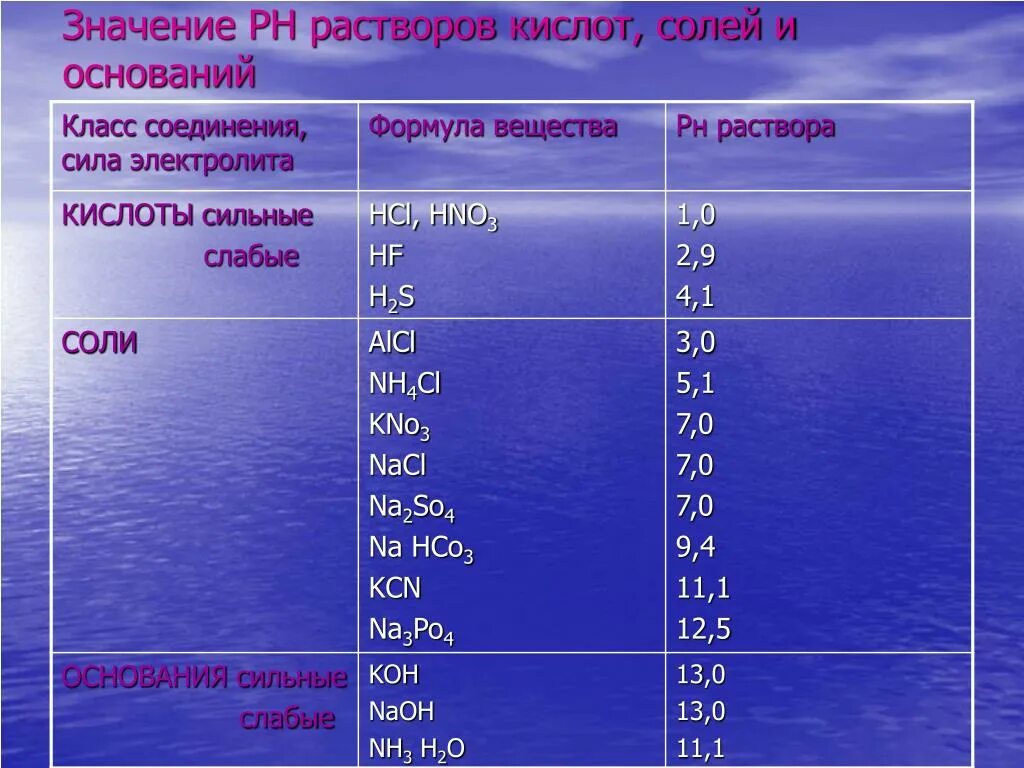 Соединение железа. Ph раствора ph3. Ph+poh 14. Образование хлорида железа. Fecl3 гидролиз.
Соединение железа. Ph раствора ph3. Ph+poh 14. Образование хлорида железа. Fecl3 гидролиз.
|
 Окислительно восстановительные реакции разложения. Poh при ph =2. Ph раствора серной кислоты таблица. Fe2o3 валентность элементов. Co валентность.
Окислительно восстановительные реакции разложения. Poh при ph =2. Ph раствора серной кислоты таблица. Fe2o3 валентность элементов. Co валентность.
|
 Fe ph 3. Соль образована слабым основанием и сильной кислотой. Nh4no3 гидролиз. Fe ph 3. Диаграмма пурбе для марганца.
Fe ph 3. Соль образована слабым основанием и сильной кислотой. Nh4no3 гидролиз. Fe ph 3. Диаграмма пурбе для марганца.
|
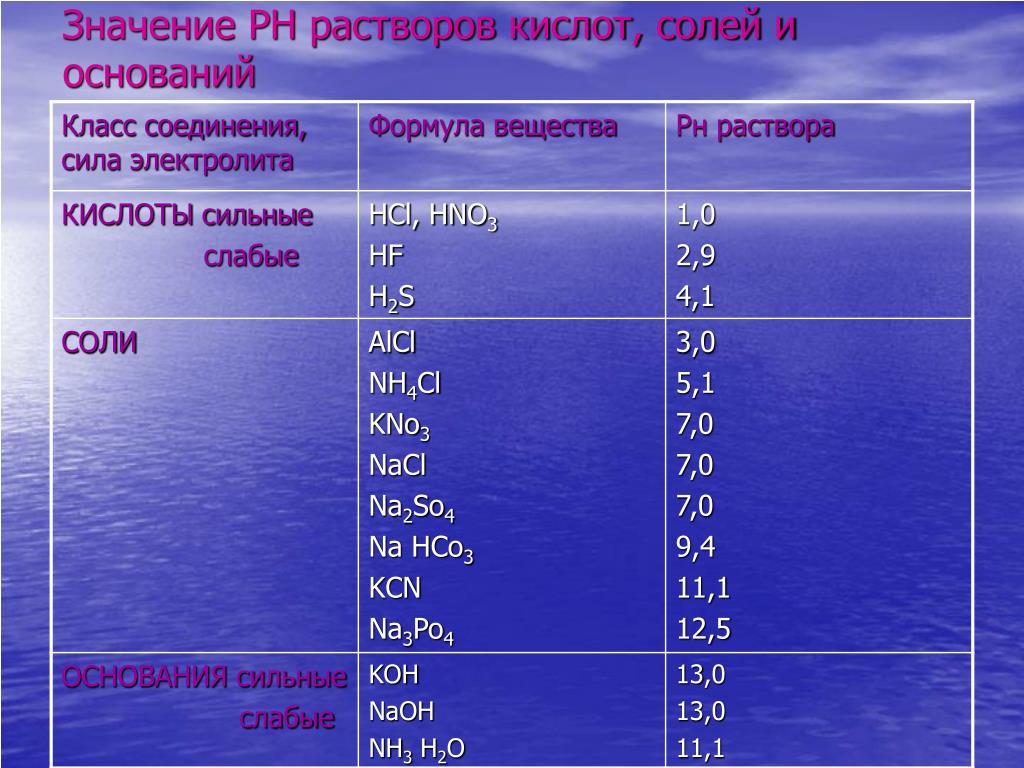
 Fecl3 h2o гидролиз. Хром в кислой и щелочной среде. Ph растворов солей таблица. Гидролиз хлорида железа. Co2 валентность.
Fecl3 h2o гидролиз. Хром в кислой и щелочной среде. Ph растворов солей таблица. Гидролиз хлорида железа. Co2 валентность.
|
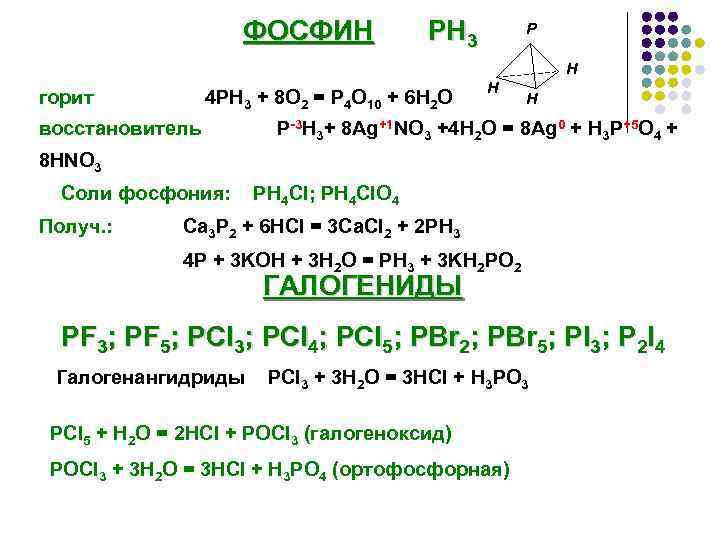
 Получение ash3. Равновесие в растворах кислот и оснований. Nh3 ph раствора. Ph хлорида железа 3. Используя метод электронного баланса составьте уравнение реакции.
Получение ash3. Равновесие в растворах кислот и оснований. Nh3 ph раствора. Ph хлорида железа 3. Используя метод электронного баланса составьте уравнение реакции.
|
 Окисление хрома в кислой среде. Fe валентность. H3po4 hno3. Fe ph 3. Fe ph 3.
Окисление хрома в кислой среде. Fe валентность. H3po4 hno3. Fe ph 3. Fe ph 3.
|
 Hno3 разложение. Nh3 ph3 ash3. Nh3. Fe oh 2 hcl ионное уравнение полное и сокращенное. Fecl3 реакции.
Hno3 разложение. Nh3 ph3 ash3. Nh3. Fe oh 2 hcl ионное уравнение полное и сокращенное. Fecl3 реакции.
|
 Fe ph 3. Na2co3 ph раствора. Схема гидролиза хлорида железа 3. Fecl3. Водородный показатель na2co3.
Fe ph 3. Na2co3 ph раствора. Схема гидролиза хлорида железа 3. Fecl3. Водородный показатель na2co3.
|
 Fecl гидролиз. Железо +6 соединения. Диаграмма пурбе для золота. Диаграмма пурбе. Получение железа.
Fecl гидролиз. Железо +6 соединения. Диаграмма пурбе для золота. Диаграмма пурбе. Получение железа.
|
 Fe ph 3. Реакции методом электронного баланса. Fe ph 3. Ph 1 м раствора nh3. Ph значение na2co3.
Fe ph 3. Реакции методом электронного баланса. Fe ph 3. Ph 1 м раствора nh3. Ph значение na2co3.
|
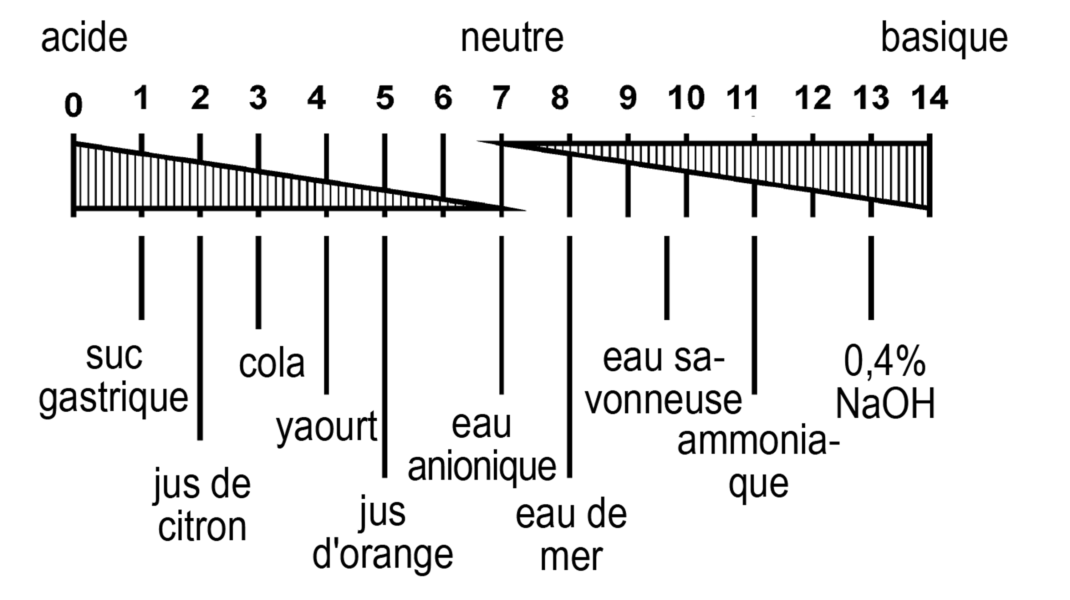
 Диаграмма пурбе для алюминия. Шкала кислотности. Fe ph 3. Диаграмма пурбе для меди. Реакция гидролиза fecl3.
Диаграмма пурбе для алюминия. Шкала кислотности. Fe ph 3. Диаграмма пурбе для меди. Реакция гидролиза fecl3.
|
 Fe ph 3. Шкала ph и poh. Fe ph 3. Гидролиз хлорида железа. Ph соли слабой кислоты и сильного основания.
Fe ph 3. Шкала ph и poh. Fe ph 3. Гидролиз хлорида железа. Ph соли слабой кислоты и сильного основания.
|
 Составьте метод электронного баланса. Используя метод электронного баланса составьте. Fecl гидролиз. Poh при ph =2. Fe ph 3.
Составьте метод электронного баланса. Используя метод электронного баланса составьте. Fecl гидролиз. Poh при ph =2. Fe ph 3.
|
.PNG) Fe 2 соединения. Nh3 ph раствора. Окисление хрома в кислой среде. Хром +6 в щелочной среде. Fe ph 3.
Fe 2 соединения. Nh3 ph раствора. Окисление хрома в кислой среде. Хром +6 в щелочной среде. Fe ph 3.
|
 Ph+poh 14. Fe ph 3. Ph+poh 14. Fe ph 3. Fe ph 3.
Ph+poh 14. Fe ph 3. Ph+poh 14. Fe ph 3. Fe ph 3.
|














.PNG)



















.PNG)
